姜黄素如何抑制癌症
来源:《PNAS》
作者:Sourav Banerjee等
时间:2018-07-18
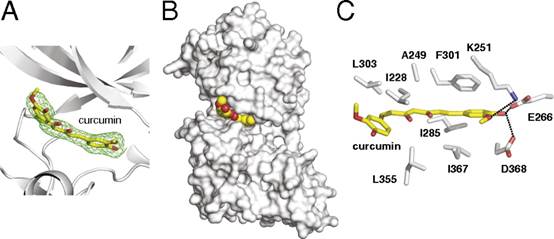
(通过X射线晶体技术获得的3D图像,图中姜黄素(黄色和红色)与激酶DYRK2结合在一起)
来自浙江大学生命科学研究院,北京大学,以及加州大学圣地亚哥分校的研究人员发表了题为“Ancient drug curcumin impedes 26S proteasome activity by direct inhibition of dual-specificity tyrosine-regulated kinase 2”的文章,通过X射线晶体学和激酶抑制剂特异性分析,他们发现一种佐料姜中天然存在的化合物:姜黄素与双特异性酪氨酸调节激酶??2(DYRK2,生物通注)能在原子水平上结合。
这种之前从未报道的姜黄素生物化学相互作用会抑制DYRK2,从而阻止细胞增殖并减轻癌症负担。这一研究发现公布在PNAS杂志上。
不过研究人员指出,单独使用姜黄素可能不是解决问题的办法。
因为一般来说,姜黄素很快被排出体外,如果姜黄素可以作为一种有效的药物,它需要进行修改才能进入血液,这样才能在体内停留足够长的时间,靶向癌症。而且由于姜黄素本身各种化学缺陷,可能不足以完全逆转癌症。
尽管姜黄素已经研究了250多年之久,之前也已经报道了其抗癌特性,但迄今为止还没有其它研究报道过姜黄素与蛋白激酶靶标结合的共晶结构。
激酶IKK和GSK3被认为是导致抗癌作用的主要姜黄素靶点,但最新研究中的姜黄素与DYRK2的共结晶结构,以及140-panel激酶抑制剂分析,表明姜黄素与DYRK2活性位点结合紧密,而后者的结合,其抑制水平比IKK或GSK3强500倍。”
利用生化,小鼠癌症模型和细胞模型,研究小组发现姜黄素是DYRK2的选择性抑制剂,这种新型分子靶标不仅具有化学敏感性,而且具有蛋白酶体抑制剂抗性/适应性癌症的抗癌潜力。
“我们的结果揭示了姜黄素在DYRK2-蛋白酶体抑制中的意外作用,并提供了一个概念验证,即蛋白酶体调节剂的药理学操作可能为难以治疗的三阴性乳腺癌和多发性骨髓瘤治疗提供新的机会。我们的主要目标是开发一种能够在患有这些癌症的患者中靶向DYRK2的化合物”,文章通讯作者之一,浙江大学生命科学研究院郭行教授说。
DYRK2消化会影响蛋白酶体的活性,表现出较慢的癌症增殖速率,降低小鼠模型中的肿瘤大小。结合FDA批准的多发性骨髓瘤药物:carfilzomib,姜黄素能诱导了更高的癌细胞死亡率,而正常的非癌细胞受到的影响较小。
这表明将蛋白酶体调节剂(如DYRK2)与蛋白酶体抑制剂结合使用可能是一种有前景的抗癌治疗方法,副作用较小,但需要进一步研究。(来源:生物通 张迪)
Ancient drug curcumin impedes 26S proteasome activity by direct inhibition of dual-specificity tyrosine-regulated kinase 2
Abstract Curcumin, the active ingredient in Curcuma longa, has been in medicinal use since ancient times. However, the therapeutic targets and signaling cascades modulated by curcumin have been enigmatic despite extensive research. Here we identify dual-specificity tyrosine-regulated kinase 2 (DYRK2), a positive regulator of the 26S proteasome, as a direct target of curcumin. Curcumin occupies the ATP-binding pocket of DYRK2 in the cocrystal structure, and it potently and specifically inhibits DYRK2 over 139 other kinases tested in vitro. As a result, curcumin diminishes DYRK2-mediated 26S proteasome phosphorylation in cells, leading to reduced proteasome activity and impaired cell proliferation. Interestingly, curcumin synergizes with the therapeutic proteasome inhibitor carfilzomib to induce apoptosis in a variety of proteasome-addicted cancer cells, while this drug combination exhibits modest to no cytotoxicity to noncancerous cells. In a breast cancer xenograft model, curcumin treatment significantly reduces tumor burden in immunocompromised mice, showing a similar antitumor effect as CRISPR/Cas9-mediated DYRK2 depletion. These results reveal an unexpected role of curcumin in DYRK2-proteasome inhibition and provide a proof-of-concept that pharmacological manipulation of proteasome regulators may offer new opportunities for anticancer treatment.
原文链接:http://www.pnas.org/content/pnas/early/2018/07/05/1806797115.full.pdf




