上海有机所在硫肽类抗生素的生物合成机制研究方面获得进展
来源:JOURNAL OF THE AMERICAN CHEMICAL SOCIETY
作者:Zhi Lin等
时间:2017-09-14
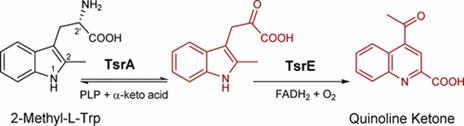
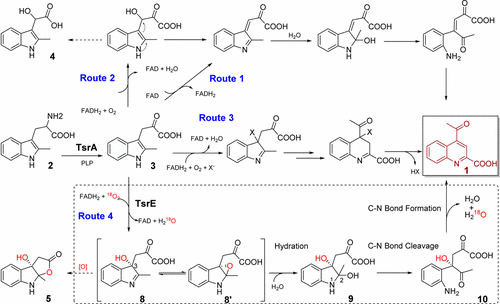
黄素依赖的加氧酶(Flavin-dependent oxygenase)是一类以黄素腺嘌呤二核苷酸或黄素单核苷酸为辅酶的氧化还原酶,在生命过程的各个阶段参与各种与氧化还原相关的生化反应。近日,中国科学院上海有机化学研究所生命有机化学国家重点实验室研究员刘文课题组和金属有机国家重点实验室研究员郭寅龙课题组合作,以硫肽类抗生素的典型代表硫链丝菌素(Thiostrepton,TSR)为研究对象,报道了一例黄素依赖的加氧酶通过底物的立体专一性氧化来促进吲哚五元环的扩环重排,揭示了自然界中一种喹啉单元形成的酶学新机制。相关成果在线发表在《美国化学会志》上。
硫肽类抗生素是一类富含元素硫、结构被高度修饰的环肽类抗生素,大多具有良好的抗菌活性。含喹萘啶酸(Quinoline acid,QA)单元的双环硫肽具备抗耐药菌活性,并具有抗癌、抗疟、抗支原体以及免疫抑制等活性,如代表性成员硫链丝菌素 TSR。刘文课题组长期从事硫肽类抗生素的生物合成机制及分子改造研究,前期研究工作证实了 QA 部分的修饰对于硫肽类抗生素的生物活性和理化性质改善十分重要。QA 的生物合成起源于 L - 色氨酸,但如何进过分子内的重排扩环反应形成关键的中间体喹啉酮(quinoline ketone)并不清楚。结合体内生物转化、体外生化验证等多种手段,研究人员发现黄素依赖的加氧酶 TsrE 能够以还原态黄素 FADH2 为辅因子,利用 O2 立体专一性地氧化中间体 2 - 甲基吲哚 -3- 丙酮酸并形成 C3 位为 S 构型的高活泼性的羟基中间体,从而诱发了包括 C - N 键的断裂和重新形成紧密偶联在内的水解开环、环化和芳构化反应,促使吲哚转化为喹啉单元;后者经过修饰与活化之后,与来源于前体肽的硫肽核心骨架整合,形成 TSR- 型双环硫肽成员所特有的侧环体系。郭寅龙课题组运用质谱分析手段,对这一不同寻常的扩环重排过程中产生的高活泼性中间体进行了捕获和鉴定。上述发现代表了色氨酸官能团化的一种新策略,丰富了有关 TSR- 型双环硫肽侧环构筑的认知,所催化的选择性氧化反应在有机化学合成中具有潜在的应用价值。这种吲哚扩环机制在自然界中可能普遍存在,如植物来源的抗疟药奎宁(Quinine)类天然产物的形成也经历了类似的选择性氧化诱发的扩环过程。
该工作得到了国家自然科学基金委、科技部、上海市科委和中科院等的资助。(来源:中国科学院上海有机化学研究所)
Processing 2-Methyl-l-Tryptophan through Tandem Transamination and Selective Oxygenation Initiates Indole Ring Expansion in the Biosynthesis of Thiostrepton
Abstract Thiostrepton (TSR), an archetypal member of the family of ribosomally synthesized and post-translationally modified thiopeptide antibiotics, possesses a biologically important quinaldic acid (QA) moiety within the side-ring system of its characteristic thiopeptide framework. QA is derived from an independent l-Trp residue; however, its associated transformation process remains poorly understood. We here report that during the formation of QA, the key expansion of an indole to a quinoline relies on the activities of the pyridoxal-5′-phosphate-dependent protein TsrA and the flavoprotein TsrE. These proteins act in tandem to process the precursor 2-methyl- l-Trp through reversible transamination and selective oxygenation, thereby initiating a highly reactive rearrangement in which selective C2–N1 bond cleavage via hydrolysis for indole ring-opening is closely coupled with C2′–N1 bond formation via condensation for recyclization and ring expansion in the production of a quinoline ketone intermediate. This indole ring-expansion mechanism is unusual, and represents a new strategy found in nature for l-Trp-based functionalization.
原文链接:http://pubs.acs.org/doi/ipdf/10.1021/jacs.7b05337




